8月10日,哈尔滨医科大学李晓波教授,美国希望之城贝克曼研究中心苏瑞教授以及北京协和医学院余佳教授团队合作在Cancer Research杂志发表了题为The IGF2BP3-COPS7B axis facilitates mRNA translation to drive colorectal cancer progression的研究成果。该研究报道了IGF2BP3-COPS7B轴可以调控结肠癌细胞中核糖体生物发生及翻译起始,并详细揭示了其调控恶性肿瘤细胞核糖体生物发生过程的关键分子及其机制。

该研究从临床样本入手,通过比较分析结肠癌及正常结肠上皮组织的转录组、蛋白质组以及翻译组学数据,发现并证实了翻译效率增加是结肠癌细胞区别于正常结肠上皮细胞的一个特征性事件。随后鉴定出COPS7B在结肠癌组织中翻译效率明显增高,蛋白水平显著增加。COPS7B是COP9信号小体的一个亚基,可通过调控泛素连接酶活性进而影响蛋白泛素化状态及降解。该研究通过免疫共沉淀-蛋白质谱技术,发现与COPS7B相互作用的蛋白其功能在核糖体和蛋白翻译过程中富集,提示COPS7B可能是一个新的核糖体互作蛋白。进一步通过多聚核糖体图谱技术及功能研究证实COPS7B定位于核糖体,并能够增强肿瘤细胞翻译。利用核糖体印迹测序技术(Ribo-seq)发现COPS7B能够特异性促进rRNA转录和加工过程中关键调控基因及核糖体蛋白编码基因的翻译,表明COPS7B是结肠癌中多层面、系统性调控核糖体生物发生的关键分子。此外,该研究还证明COPS7B能够促进mTOR的翻译并增加其蛋白产量,进而通过mTOR依赖的方式促进翻译起始过程。因此COPS7B不仅增加核糖体数量,而且提升其翻译效率,进而增强结肠癌细胞中的蛋白合成。最后,该研究还发现RNA结合蛋白IGF2BP3的表达升高是结肠癌中COPS7B翻译效率上调的重要原因。而且IGF2BP3和COPS7B相似的功能和作用机制,证明IGF2BP3是COPS7B的功能性上游调控分子。
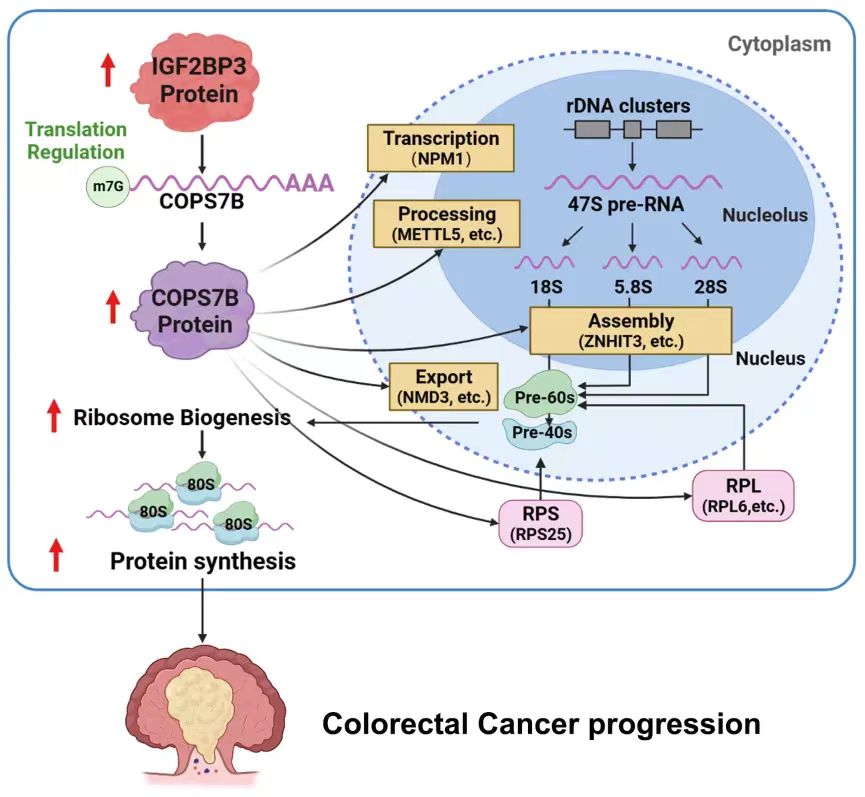
该研究不仅揭示了由IGF2BP3-COPS7B构成的调控轴促进结肠癌细胞核糖体生物发生的作用和机制,而且证明IGF2BP3和COPS7B能够驱动结肠癌演进,从而为结肠癌的防治提供了新靶点。
原文链接:https://doi.org/10.1158/0008-5472.CAN-23-0557